Es Termodinamica 2020 2021 pt3 - Corso di TERMODINAMICA A. 20 20 / Esercizi per l'esame – parte III - Studocu
Riassunto esame Chimica inorganica, Prof. D'andrea Luca Domenico, libro consigliato Chimica: Un approccio molecolare, Nivaldo J. Tro
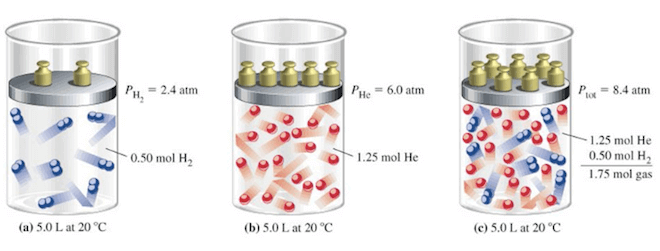
LEGGE DI DALTON: In volume due gas perfetti si comportano come se l'altro non ci fosse (Questo è dovuto al fatto che in un gas perfetto le dimensioni delle molecole sono molto
Corso di TERMODINAMICA A.A. 2019/2020 Esercizi per l'esame – parte III 1. Un beaker contiene 1.3 lbm di HCl: quante lb-mol c

Esercizio n. 1 Un gas perfetto è costituito da atomi di massa molare M = 50 g/mol e le cui molecole hanno velocità quadratica media uguale a 380 m/s. - ppt scaricare

Esercizio n. 1 Un gas perfetto è costituito da atomi di massa molare M = 50 g/mol e le cui molecole hanno velocità quadratica media uguale a 380 m/s. - ppt scaricare
VOLUMI MOLARI REALI DEI GAS ( correzione del volume molare ideale di Avogadro) - EnergeticAmbiente.it